La clorexidina gluconato (CHG) rappresenta uno dei biocidi più impiegati in ambito sanitario, disponibile in formulazioni acquose (0,05%–4%) e alcoliche (0,5%–2% in isopropanolo 70%).
Nonostante la sua elevata efficacia, la pressione selettiva esercitata dall'uso prolungato e spesso subottimale di CHG ha favorito l'emergenza di fenotipi microbici con ridotta sensibilità o vera resistenza. Il presente articolo esamina sistematicamente i meccanismi molecolari e fenotipici alla base della resistenza, con particolare attenzione ai patogeni implicati nelle Infezioni Correlate all'Assistenza (ICA).
1. Premessa: meccanismo d'azione della Clorexidina Gluconato
La CHG è una biguanide dicationica che esercita la propria attività biocida attraverso un'interazione elettrostatica con la membrana cellulare batterica, carica negativamente.
L'affinità per i fosfolipidi anionici e per i lipopolisaccaridi (nei gram-negativi) determina una sequenza di eventi dose-dipendente:
- a basse concentrazioni (≤0,01–0,06%): effetto batteriostatico per inibizione dell'attività enzimatica e alterazione del potenziale di membrana;
- a concentrazioni intermedie (0,1–0,5%): danno alla membrana citoplasmatica con fuoriuscita di componenti intracellulari a basso peso molecolare (ioni K⁺, ATP);
- ad alte concentrazioni (≥1–2%): precipitazione e coagulazione del citoplasma con effetto battericida rapido e irreversibile.
Le formulazioni alcoliche sfruttano la sinergia tra CHG e isopropanolo, che accelera la penetrazione nelle membrane lipidiche e amplia lo spettro d'azione verso virus lipofili e micobatteri non tubercolari.
2. Principi di resistenza microbica alla Clorexidina
La resistenza alla CHG non è monogenica né univoca: si tratta di un fenomeno multifattoriale che si articola in meccanismi intrinsechi — propri della biologia della specie batterica — e meccanismi acquisiti, emergenti sotto pressione selettiva.
2.1 Resistenza intrinseca
2.1.1 Ridotta permeabilità della membrana esterna (Gram-negativi)
Nei batteri gram-negativi, la membrana esterna costituisce una barriera fisica che limita la diffusione della CHG verso la membrana citoplasmatica. Il lipopolisaccaride (LPS) è il principale ostacolo: modificazioni della sua composizione (variazioni nei lipidi A, riduzione dei gruppi fosfato, sostituzione con aminoarabinoso o fosfatidiletanolammina) riducono la carica negativa superficiale e quindi l'attrazione elettrostatica con la molecola dicationica. Questa strategia è documentata in Klebsiella pneumoniae, Pseudomonas aeruginosa e Acinetobacter baumannii.
2.1.2 Struttura della parete cellulare (Gram-positivi)
Nei gram-positivi, gli acidi teicoici carichi negativamente del peptidoglicano legano elettrostaticamente la CHG, riducendo la quantità di molecola che raggiunge la membrana citoplasmatica. Staphylococcus aureus può modulare la carica superficiale attraverso la D-alaninazione degli acidi teicoici (gene dltABCD), riducendo così l'affinità per la CHG.
2.1.3 Parete micoide e biofilm
La produzione di esopolisaccaridi extracellulari e la formazione di biofilm rappresentano una delle forme più potenti di resistenza intrinseca. All'interno del biofilm:
- la matrice di EPS ostacola la diffusione della CHG;
- le cellule in stato quiescente (persister cells) esprimono metabolismi ridotti, rendendosi insensibili ai biocidi che agiscono su processi metabolici attivi;
- il gradiente di ossigeno e nutrienti genera sottopopolazioni fenotipicamente eterogenee con differenti livelli di tolleranza.
Questo meccanismo è particolarmente rilevante per Staphylococcus epidermidis, Pseudomonas aeruginosa e Candida albicans.
2.2 Resistenza acquisita
2.2.1 Pompe di efflusso
Il meccanismo più documentato e clinicamente rilevante è l'iperattivazione di pompe di efflusso transmembranarie, che espellono attivamente la CHG prima che raggiunga una concentrazione intracellulare battericida.
Le principali famiglie coinvolte sono:
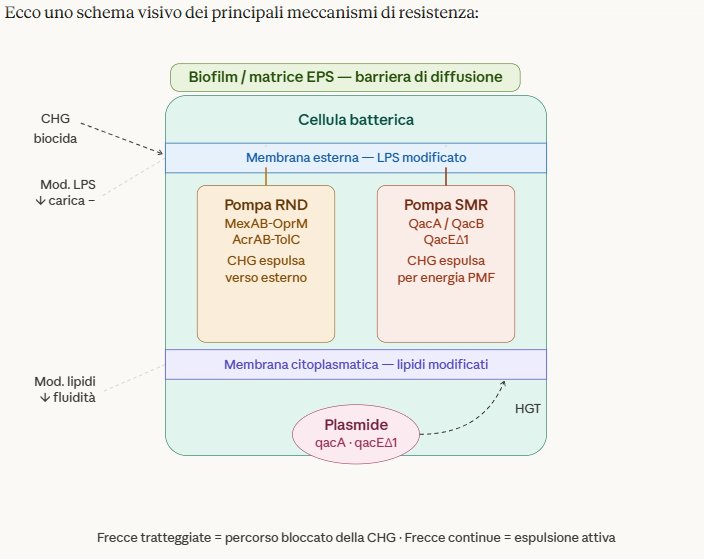
Famiglia MATE (Multidrug And Toxin Extrusion) — la pompa QacA e la correlata QacB (codificate da plasmidi in S. aureus) sono tra le più studiate. QacA presenta una specificità di substrato ampia che include CHG, benzalconio cloruro e acridine, ed è trasportata da elementi mobili (plasmidi pSK1-like), facilitandone la diffusione orizzontale.
Famiglia SMR (Small Multidrug Resistance) — le proteine QacC/QacD/QacE/QacEΔ1 sono piccole proteine di membrana (circa 107 aminoacidi) che conferiscono resistenza a composti biscationici. QacEΔ1 è particolarmente preoccupante perché inserita negli integróni di classe 1, spesso co-localizzata con geni di resistenza agli antibiotici.
Famiglia RND (Resistance-Nodulation-Division) — nei gram-negativi, i sistemi tripartiti come MexAB-OprM (in P. aeruginosa), AdeABC (in A. baumannii) e AcrAB-TolC (in Enterobacterales) esportano CHG attraverso la membrana esterna, operando contro gradiente grazie all'energia del potenziale protonico.
2.2.2 Modificazione del bersaglio
La CHG non ha un singolo bersaglio molecolare discreto, il che limita teoricamente questa strategia; tuttavia, la modificazione della composizione lipidica della membrana (aumento degli acidi grassi con catene più lunghe o sature, variazioni nel rapporto fosfatidilglicerolo/cardiolipina) riduce la fluidità e la permeabilità, diminuendo l'efficacia di penetrazione della molecola biocida.
2.2.3 Degradazione enzimatica
Alcune specie batteriche, in particolare micobatteri ambientali e Pseudomonas spp., producono enzimi in grado di degradare parzialmente la molecola di CHG o di sequestrarne i cationi, riducendone la biodisponibilità. Questo meccanismo è ad oggi meno caratterizzato rispetto alle pompe di efflusso, ma è oggetto di ricerca attiva.
2.2.4 Resistenza adattativa e tolleranza
Distinta dalla vera resistenza (fenotipo stabile e trasmissibile), la tolleranza adattativa è una risposta transitoria e dose-dipendente: esposizioni ripetute a concentrazioni sub-letali di CHG inducono l'upregolazione di geni di risposta allo stress (famiglie clp, groEL, dnaK) e delle pompe di efflusso. Una volta rimossa la pressione selettiva, il fenotipo può tornare alla suscettibilità basale, ma in presenza di pressione selettiva continua la tolleranza può stabilizzarsi geneticamente.
2.2.5 Trasferimento orizzontale di geni (HGT)
I geni qac (in particolare qacA, qacB, qacEΔ1) sono localizzati su elementi genetici mobili — plasmidi coniugativi, integróni, trasposoni — che ne consentono la diffusione orizzontale inter- e intra-specie, anche in assenza di pressione selettiva diretta da CHG.
La co-localizzazione con geni di resistenza agli antibiotici sugli stessi elementi mobili (co-selezione) implica che l'uso di antibiotici può selezionare indirettamente la resistenza alla CHG e viceversa.
3. Batteri resistenti responsabili di ICA
L'elenco seguente comprende i principali patogeni per i quali è documentata una riduzione significativa della suscettibilità alla CHG in contesti di assistenza sanitaria, con indicazione dei meccanismi prevalenti e del correlato rischio di ICA.
3.1 Staphylococcus aureus meticillino-resistente (MRSA)
È il patogeno per cui la correlazione CHG–resistenza è meglio caratterizzata. La presenza dei geni qacA/B su plasmidi pSK1-like è documentata in ceppi MRSA ospedalieri con frequenza variabile tra il 20% e il 60% nei diversi studi.
La co-residenza sul medesimo plasmide di geni mecA (resistenza alla meticillina) e qacA/B configura un classico scenario di co-selezione. I ceppi con qacA/B-positivi mostrano MIC (Minimum Inhibitory Concentration) alla CHG 4–8 volte superiori ai ceppi sensibili. Responsabile di infezioni della ferita chirurgica, batteriemia, endocardite e polmonite associata a ventilazione meccanica (VAP).
3.2 Staphylococcus epidermidis e Stafilococchi Coagulasi-Negativi (CoNS)
I CoNS, commensali cutanei ubiquitari, sono i principali patogeni delle ICA correlate a dispositivi intravascolari (CVC, cateteri arteriosi, PICC). S. epidermidis è un produttore prolificatico di biofilm (geni icaABCD) ed è tra i batteri con la più elevata prevalenza di geni qac (fino al 70% in alcuni contesti di terapia intensiva). La CHG a basse concentrazioni esercita su questi ceppi effetto subletale, favorendo la selezione di varianti con fenotipo qac-amplificato.
3.3 Enterococcus faecalis ed Enterococcus faecium VRE
Gli enterococchi vancomicino-resistenti (VRE) mostrano ridotta permeabilità di membrana e producono biofilm particolarmente resistente alla penetrazione dei biocidi.
La MIC alla CHG nei VRE può essere significativamente più elevata rispetto a ceppi sensibili, e la co-selezione tra resistenza agli antibiotici glicopeptidici e ridotta suscettibilità alla CHG è stata documentata in unità di trapianto e oncoematologiche. Responsabili di infezioni urinarie, endocarditi e peritoniti in pazienti immunocompromessi.
3.4 Klebsiella pneumoniae (inclusi ceppi KPC e NDM)
K. pneumoniae sfrutta principalmente la ridotta permeabilità della membrana esterna (variazioni delle porine OmpK35/OmpK36, modificazione dell'LPS) e i sistemi di efflusso RND (in particolare AcrAB-TolC) per ridurre la suscettibilità alla CHG. I ceppi produttori di carbapenemasi (KPC, NDM, OXA-48) mostrano frequentemente un fenotipo di ridotta suscettibilità alla CHG, configurando un'emergenza clinica critica per le ICA in terapia intensiva, con mortalità associata superiore al 40%.
3.5 Pseudomonas aeruginosa
Caratterizzato da una membrana esterna con bassissima permeabilità intrinseca e da molteplici sistemi di efflusso RND (MexAB-OprM, MexCD-OprJ, MexEF-OprN, MexXY-OprM), P. aeruginosa è intrinsecamente tollerante alla CHG a concentrazioni usuali. La sua capacità di formare biofilm persistente su cateteri, ventilatori e superfici ambientali ne fa un protagonista delle infezioni correlate a dispositivi, VAP e infezioni del sito chirurgico in pazienti con ustioni o fibrosi cistica.
3.6 Acinetobacter baumannii
Patogeno opportunista di elezione nelle terapie intensive, A. baumannii combina la riduzione/assenza delle porine (OmpA, CarO) con l'iperattivazione del sistema di efflusso AdeABC, raggiungendo livelli di tolleranza alla CHG documentati anche a concentrazioni comunemente impiegate per le decontaminazioni topiche. I ceppi pan-resistenti agli antibiotici (PDRAB) rappresentano una sfida terapeutica e un rischio ICA di massima gravità.
3.7 Enterobacter cloacae e altri Enterobacterales
Nell'ambito degli Enterobacterales, oltre a K. pneumoniae, ceppi di Enterobacter cloacae, Serratia marcescens ed Escherichia coli produttori di ESBL o carbapenemasi hanno mostrato aumentate MIC alla CHG in studi clinici, prevalentemente mediate da pompe di efflusso AcrAB-TolC e da integróni di classe 1 portatori di qacEΔ1.
3.8 Burkholderia cepacia Complex
Il complesso B. cepacia (Bcc) presenta una membrana esterna costitutivamente poco permeabile e pompe di efflusso RND altamente attive. La resistenza intrinseca alla CHG è tanto pronunciata da rendere la molecola sostanzialmente non efficace a concentrazioni usuali. Patogeno emergente nelle unità di fibrosi cistica e nelle UCI, è responsabile di batteriemie fatali con materiale contaminato da CHG già documentate in letteratura (episodi legati a flaconi di colliri e prodotti per lavaggio delle mani contaminati alla produzione).
3.9 Candida spp. (agente patogeno fungino)
Pur non essendo un batterio, Candida albicans e Candida parapsilosis meritano menzione: la struttura della parete cellulare fungina (β-glucani, mannani, chitina) riduce la penetrazione della CHG, e il biofilm fungino mostra una resistenza al biocida 50–100 volte superiore alle cellule planctoniche. Il rischio ICA è rappresentato in particolare dalle candidemie correlate a CVC.
4. Implicazioni cliniche e raccomandazioni per la pratica infermieristica
La comprensione dei meccanismi di resistenza ha dirette implicazioni operative nell'assistenza infermieristica:
Concentrazione efficace: Le formulazioni con CHG al 2% in alcol 70% mantengono la massima efficacia grazie all'azione sinergica; le soluzioni acquose diluenti (≤0,05%) non devono essere impiegate per la decontaminazione cutanea preoperatoria o per i siti di inserzione dei dispositivi intravascolari.
Tempo di contatto: Le linee guida CDC e SHEA raccomandano un tempo di contatto di almeno 30 secondi per la disinfezione cutanea, con completa asciugatura prima dell'inserzione del dispositivo; la fretta applicativa riduce la concentrazione effettiva e favorisce la selezione adattativa.
Rotazione dei biocidi: In unità ad alto rischio, l'alternanza programmata tra CHG e altri biocidi (iodopovidone, ipoclorito) può ridurre la pressione selettiva cumulativa, sebbene le evidenze di efficacia clinica siano ancora oggetto di studio.
Sorveglianza microbiologica: Il monitoraggio delle MIC alla CHG nei ceppi isolati nei contesti di ICA dovrebbe essere parte integrante dei programmi di sorveglianza e controllo delle infezioni (IPC), analogamente a quanto avviene per la resistenza antibiotica.
5. Conclusioni
La resistenza alla clorexidina gluconato è un fenomeno biologicamente complesso, mediato da meccanismi molecolari diversificati — pompe di efflusso, modificazione della membrana, biofilm, trasferimento genico orizzontale — e clinicamente rilevante per la gestione delle ICA.
I principali patogeni coinvolti (MRSA, CoNS, VRE, K. pneumoniae KPC, P. aeruginosa, A. baumannii, Bcc) coincidono in larga misura con quelli della lista ESKAPE dell'OMS, sottolineando la necessità di un approccio integrato ai programmi di stewardship dei biocidi, parallelo a quello degli antibiotici.
Bibliografia
- McDonnell G, Russell AD. Antiseptics and Disinfectants: Activity, Action, and Resistance. Clinical Microbiology Reviews. 1999;12(1):147–179.
- Kampf G. Acquired Resistance to Chlorhexidine — Is It Time to Establish an 'Antiseptic Stewardship' Initiative? Journal of Hospital Infection. 2016;94(3):213–227.
- Maillard JY, Kampf G, Cooper R. Antimicrobial Stewardship of Antiseptics That Are Relevant to Wounds: The Need for a New Approach. JAC-Antimicrobial Resistance. 2021;3(1):dlaa105.
- Poole K. Mechanisms of Bacterial Biocide and Antibiotic Resistance Overlap. Symposium Series (Society for Applied Microbiology). 2002;(31):55S–64S.
- Cieplik F, et al. Resistance Toward Chlorhexidine in Oral Bacteria — Is There Cause for Concern? Frontiers in Microbiology. 2019;10:587.
- Hardy KJ, Oppenheim BA, Gossain S, Gao F, Hawkey PM. A Study of the Relationship Between Environmental Contamination with MRSA and Patients' Hand Carriage. Journal of Hospital Infection. 2006;65(1):59–67.
- Lee AS, et al. Methicillin-resistant Staphylococcus aureus. Nature Reviews Disease Primers. 2018;4:18033.
- Gould IM. The Problem of Hospital-Acquired Meticillin-Resistant Staphylococcus aureus and Antiseptic Resistance. Journal of Hospital Infection. 2011;79(4):292–296.
- WHO. Global Priority List of Antibiotic-Resistant Bacteria to Guide Research, Discovery, and Development of New Antibiotics. Ginevra: World Health Organization; 2017.
- Hernández A, et al. Biocide–Antibiotic Resistance Co-selection: Mechanisms and Clinical Implications. Current Opinion in Microbiology. 2021;64:60–67.
- CDC/HICPAC. Guidelines for the Prevention of Intravascular Catheter-Related Infections. Atlanta: Centers for Disease Control and Prevention; 2011 (aggiornamento 2017).
- ECDC. Surveillance of Healthcare-Associated Infections in Europe. Stoccolma: European Centre for Disease Prevention and Control; 2023.
- Brooke JS. Stenotrophomonas maltophilia: An Emerging Global Opportunistic Pathogen. Clinical Microbiology Reviews. 2012;25(1):2–41. (incluso per il confronto con Bcc)
- Nseir S, et al. Chlorhexidine Bathing and Ventilator-Associated Pneumonia. Lancet. 2015;386(9992):421–423.
Il documento è stato realizzato da claude.ai nella versione free, il prompt inserito è: Il disinfettante clorexidina gluconato è disponibile in varie concentrazioni e formulazioni con alcol. Scrivi i principi di resistenza al disinfettante da parte dei microrganismi, elenca i batteri resistenti responsabili di ICA.


