La fibrillazione atriale e il flutter atriale sono tra le più comuni aritmie atriali, le quali a loro volta sono un gruppo eterogeneo di aritmie sopraventricolari.
Il flutter atriale è molto comune ed è caratterizzata da un ritmo cardiaco anormale con una frequenza atriale di 300 battiti/min e una frequenza ventricolare che può essere fissa o variabile causando palpitazioni, affaticamento e una sincope.
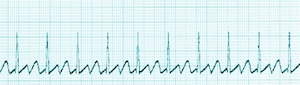
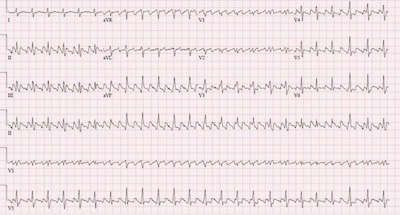
Il flutter atriale è una tachicardia macro-rientrante e, a seconda della sede di origine, può essere un flutter atriale tipico o atipico. I reperti elettrocardiografici del flutter atriale sono onde di flutter senza una linea isoelettrica tra il complesso QRS.
L'asse elettrico delle onde del flutter può aiutare a determinare l'origine del flutter atriale.
Il flutter può essere tipico, chiamato anche dipendente dall'istmo cavotricuspide (CTI) ed è il tipo più comune di flutter atriale.
Questo ritmo ha origine nell'atrio destro a livello della valvola tricuspide ed è visto nell'elettrocardiogramma come modulazione negativa continua nelle derivazioni inferiori (II, III e AVF) e deflessioni atriali piatte nelle derivazioni I e aVL.
Il flutter atriale atipico è indipendente dalla CTI e l'origine dell'aritmia può essere nell'atrio destro o nell'atrio sinistro.
Meno comunemente, l'attivazione atriale può essere in senso orario, e quindi l'aspetto elettrocardiografico è diverso e non è possibile differenziarlo facilmente dal flutter atriale non dipendente dall'istmo.
Epidemiologia
Il flutter atriale è la seconda aritmia cardiaca più comune dopo la fibrillazione atriale e spesso sono anche associati, ma l'incidenza e la prevalenza del flutter atriale sono meno note rispetto alla fibrillazione atriale.
Il flutter atriale è comune nei pazienti con malattie sottostanti come:
- broncopneumopatia cronica ostruttiva,
- ipertensione polmonare,
- insufficienza cardiaca.
Mentre il flutter atriale isolato in assenza di un anormale anatomia cardiaca, è raro e di solito è presente quando si sono sviluppate anomalie delle dimensioni atriali.
Il flutter atriale è più frequente nei maschi che nelle femmine e l'invecchiamento è un fattore di rischio significativo.
Storia e fisica
I pazienti con flutter atriale possono essere asintomatici o presentare sintomi quali:
- palpitazioni,
- stordimento,
- affaticamento,
- mancanza di respiro soprattutto in presenza di conduzione ventricolare rapida.
La diminuzione della tolleranza all'esercizio è un altro sintomo che può essere presente durante la valutazione del paziente.
Durante la frequenza ventricolare rapida, nei pazienti suscettibili con frequenze ventricolari elevate possono verificarsi anche ipotensione, sincope e quasi sincope.
Alcuni pazienti rimangono asintomatici fino a quando non sviluppano insufficienza cardiaca acutamente scompensata, cardiomiopatia indotta da tachicardia e ictus embolico.
L'esame obiettivo nei pazienti con flutter atriale mostrerà polso periferico regolare o irregolarmente regolare (a causa della conduzione variabile dal nodo atrioventricolare), distensione venosa giugulare, suoni respiratori con crepitii nei campi polmonari, tachicardia, distensione addominale ed edema degli arti inferiori in caso di congestione si verifica.
Valutazione
L'elettrocardiogramma mostra generalmente onde di flutter con assenza di una linea isoelettrica tra i complessi QRS, con un'onda atriale di circa 300 battiti al minuto con conduzione ventricolare che può essere 2 a 1, 3 a 1 o 4 a 1 o con conduzione variabile dovuta al fenomeno di Wenckebach.
Nelle derivazioni inferiori, le tipiche onde svolazzanti assomigliano a una staccionata o a un dente di sega perché le onde P sono negative a causa della direzione del vettore.
Il tipico flutter atriale con attivazione in senso antiorario mostrerà derivazioni inferiori con onde di flutter negative con bassa ampiezza nell'elettrocatetere e le onde di flutter verticali in aVL.
Valutazione di laboratorio
È necessaria una determinazione iniziale dei fattori scatenanti del flutter atriale e una valutazione di laboratorio di:
- disturbi elettrolitici,
- funzionalità tiroidea anormale,
- infezioni,
- anemia,
- ipossia.
La correzione di queste anomalie può migliorare i sintomi e diminuire la soglia di sviluppo del flutter atriale e della rapida risposta ventricolare.
Il test di funzionalità polmonare potrebbe essere necessario per questo gruppo di pazienti; esiste una correlazione tra malattia polmonare e presenza di aritmie atriali compreso il flutter atriale.
La gestione della condizione polmonare sottostante può migliorare il controllo del flutter atriale.
Trattamento/Gestione
La gestione del trattamento dovrebbe concentrarsi sui seguenti aspetti:
-
Controllo del ritmo
-
Controllo della tariffa
-
Anticoagulazione a causa del rischio di embolizzazione
1 . Controllo del ritmo
Il mantenimento del ritmo sinusale o la conversione del ritmo sinusale è essenziale.
La persistenza del flutter atriale, può causare un rimodellamento cronico dell'atrio e rendere più difficile la gestione della frequenza e la conversione o il mantenimento del ritmo sinusale.
Esistono diversi modi per ottenere il ritmo sinusale: con cardioversione elettrica, cardioversione farmacologica e infine con ablazione transcatetere.
La strategia del ritmo si divide in gestione acuta e a lungo termine.
In ambito acuto, nei pazienti con flutter atriale che sono emodinamicamente instabili, è indicata la cardioversione sincronizzata per la conversione del ritmo sinusale per stabilizzare il paziente. [15]
Nei pazienti stabili, la cardioversione farmacologica è realizzabile con diversi antiaritmici come:
- amiodarone,
- classe IA (procainamide, chinidina e disopiramide),
- farmaci IC (flecainide e propafenone),
- calcio-antagonisti (verapamil, diltiazem),
- beta-bloccanti (metoprololo, carvedilolo, esmololo) sono alcune delle scelte per cardioversione farmacologica.
Nonostante le molteplici opzioni farmacologiche, il controllo e la conversione del flutter atriale in ritmo sinusale è difficile.
Il meccanismo attraverso il quale i farmaci antiaritmici mantengono il ritmo sinusale è la prevenzione dei battiti prematuri che di solito avviano l'attivazione del circuito tachicardico da parte di un battito rientrante o ectopico.
In presenza di una nuova diagnosi di flutter atriale, si dovrebbe iniziare il paziente con la terapia anticoagulante.
In assenza di trombo intracardiaco, può essere presa in considerazione la cardioversione elettrica in pazienti stabili, soprattutto per prevenire la persistenza dell'aritmia e l'ulteriore fibrosi che perpetuerà la presenza di flutter atriale e più difficile da controllare o convertire in ritmo sinusale.
Nei pazienti che hanno una controindicazione a questi farmaci o non li tollerano può prendere in considerazione l'ablazione con catetere del circuito del flutter atriale.
L'ablazione con catetere a radiofrequenza della CTI è il trattamento standard per il tipico flutter atriale con una percentuale di successo del 95% con poche complicanze post-procedura.
La procedura consiste nel posizionamento di cateteri intracardiaci nel seno coronarico, nell'atrio e in un catetere per ablazione.
Il target anatomico per il CTI si trova attraverso una tecnica di mappatura e intrappolamento.
Successivamente, la lesione lineare viene realizzata dal catetere di ablazione con l'utilizzo di energia a radiofrequenza.
Al termine dell'ablazione, quando la linea è completa, viene eseguita la verifica del blocco della conduzione bidirezionale e dell'assenza di flutter atriale per confermare che l'ablazione è completa.
Nei rari casi di insuccesso farmacologico e ablazione, l'ablazione del nodo atrioventricolare con il posizionamento di un pacemaker potrebbe essere indicata per prevenire la conduzione da atriale a ventricolare del flutter atriale rapido.
2 . Controllo della tariffa
Il controllo della frequenza è ottenibile con l'uso di agenti nodali atrioventricolari come calcio-antagonisti (prima linea) o beta-bloccanti. [20] La digossina è un'altra opzione per il controllo della velocità, ma deve essere usata con attenzione a causa dei suoi effetti collaterali e della sua tossicità.
La combinazione di questi agenti è un'opzione.
Un controllo adeguato del flutter atriale attraverso agenti nodali AV è difficile perché il flutter atriale si attiva continuamente alla stessa frequenza nel nodo AV.
L'obiettivo della frequenza cardiaca dovrebbe essere inferiore a 110 battiti al minuto [21], determinato dopo lo studio RACE II (Rate Control Efficacy in Permanent Atrial Fibrillation: a Comparison between Lenient versus Strict Rate Control II).
Questo studio ha confrontato un controllo rigoroso della frequenza cardiaca <80 bpm rispetto a <110 bpm, questo studio ha dimostrato che un controllo della frequenza cardiaca molto rigoroso non è necessario e un controllo più clemente riduce la polifarmacia e meno effetti collaterali e meno visite ambulatoriali.
Questo studio è stato condotto su pazienti con flutter atriale, ma può essere estrapolato al controllo della frequenza del flutter atriale.
Nei pazienti che sono intolleranti ai farmaci o hanno una bradicardia significativa a causa delle misure di controllo della frequenza, un'ablazione con catetere è un'opzione.
3. Anticoagulazione a causa del rischio di eventi embolici:
I pazienti con flutter atriale hanno un rischio di ictus simile a quelli con fibrillazione atriale. [22] L'uso di un sistema di punteggio per determinare il rischio annuale di ictus deve essere utilizzato come il CHADS2-Vasc. [23]
Questo sistema di punteggio aiuta a stratificare il rischio del paziente in base al rischio di sviluppare ictus embolico a causa di flutter atriale o fibrillazione atriale.
La presenza di insufficienza cardiaca congestizia, ipertensione sistemica, diabete, sesso femminile, età compresa tra 65 e 74 anni e una storia di malattia vascolare periferica valutano come un punto per ogni comorbidità presente.
L'età superiore a 75 anni e una storia di ictus sono due punti aggiuntivi ciascuno.
La presenza di un punto può dare al paziente un rischio annuo dell'1,3% di ictus embolico quando due punti il rischio è del 2,2%.
Nei pazienti con due o più punti, l'uso di anticoagulanti è una forte raccomandazione. Nei pazienti con un punto, si può usare l'aspirina o l'anticoagulazione completa.
Diagnosi differenziale
-
Fibrillazione atriale: per lo più irregolare, nessuna evidenza di attività atriale organizzata nell'elettrocardiogramma, assenza di onde P
-
Tachicardia atriale multifocale: morfologia di onde P multiple dovute alla presenza di più pacer atriali
-
Tachicardia atriale a conduzione variabile: la linea isoelettrica tra complessi QRS
Prognosi
La prognosi dei pazienti con flutter atriale tipico sottoposti ad ablazione con catetere è buona con un tasso di recidiva inferiore al 5%.
La persistenza del flutter atriale può generare tachicardia indurre cardiomiopatia difficile da controllare causando molteplici ricoveri per scompenso.
Complicazioni
La complicanza più comune del flutter atriale è l'aumento del rischio di ictus embolico e disabilità correlata a questo evento. L'instabilità emodinamica è anche possibile soprattutto nei pazienti con una risposta ventricolare rapida.
La cronicità e lo scarso controllo del flutter atriale possono generare tachicardia indurre cardiomiopatia e possono anche produrre insufficienza cardiaca difficile da controllare.
Le complicanze secondarie all'uso di farmaci antiaritmici sono legate al tipo di farmaco e al meccanismo alla base del farmaco.
Le complicanze dell'ablazione del flutter atriale dipendono anche dal lato dell'origine del flutter atriale.
Il flutter atriale destro è correlato a un minor numero di complicanze rispetto all'ablazione del flutter atriale sinistro, e ciò è dovuto alla necessità di creare una comunicazione transettale durante la procedura per raggiungere i fuochi dell'aritmia dell'atrio sinistro ed eseguire l'ablazione.
La puntura transettale produce una comunicazione transitoria tra le camere sinistra e destra del cuore.
C'è anche un aumento del rischio di ictus embolico con l'ablazione del flutter atriale sul lato sinistro rispetto alle procedure sul lato destro.
Migliorare i risultati del team sanitario
Non esiste una cura per il flutter atriale ed è noto che il disturbo è associato ad un alto rischio di ictus e altri fenomeni embolici; per questo la gestione del flutter atriale viene eseguita al meglio da un team interprofessionale che includa medici, specialisti, farmacista e un infermiere specializzato in cardiologia.
Mentre il cardiologo può iniziare il trattamento iniziale, la maggior parte dei pazienti è seguita dal fornitore primario o dall'infermiere.
Questi pazienti necessitano di un follow-up per tutta la vita perché esiste il rischio di un ictus embolico. Se il disturbo riceve una terapia inadeguata, porta a una scarsa qualità della vita.
I fornitori di cure primarie, i farmacisti e gli infermieri dovrebbero imporre la conformità ai farmaci.
Quei pazienti che assumono warfarin dovrebbero avere un consulto dietetico perché un improvviso cambiamento nel consumo di verdure a foglia verde può influenzare l'INR.
L'infermiere e il farmacista di ematologia devono monitorare l'INR ma l'adeguamento della dose di warfarin deve essere effettuato dal medico. Ad ogni visita clinica, deve essere eseguito un ECG e il paziente esaminato per qualsiasi fenomeno embolico.
Per migliorare i risultati, è essenziale una comunicazione aperta tra i membri del team interprofessionale.
Risultati
Nonostante i progressi nel trattamento, le recidive e i ricoveri multipli in ospedale sono molto comuni.
Figura
Flutter atriale. Contributo di Dhaval Desai, MD
Riferimenti
Author Information
Last Update: August 11, 2021.
This book is distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/), which permits use, duplication, adaptation, distribution, and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, a link is provided to the Creative Commons license, and any changes made are indicated.